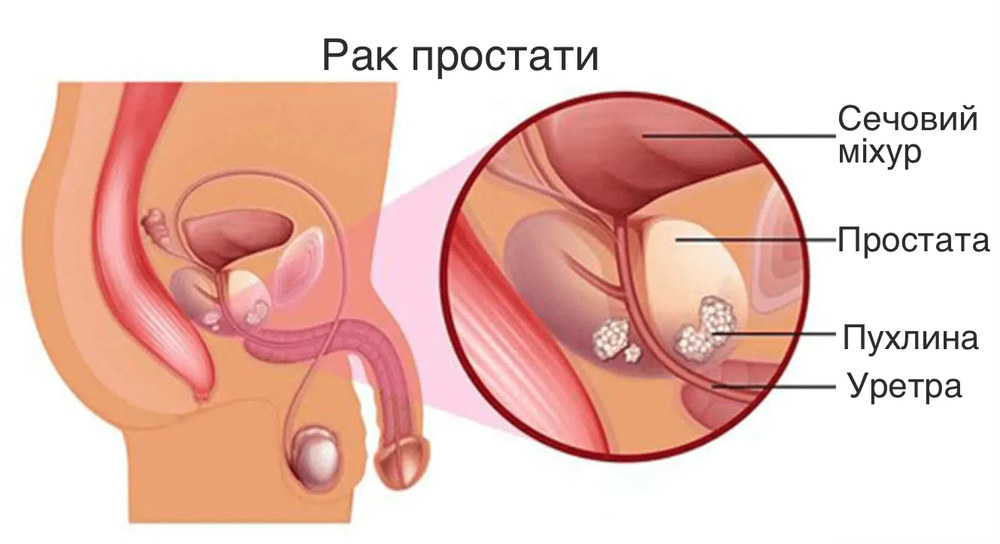
Рак простати займає провідне місце серед онкологічних захворювань у чоловіків і є другою за частотою причиною смерті від раку після раку легенів. Щорічно у світі діагностується понад 1,3 мільйона нових випадків цього захворювання. В Україні рак простати посідає третє місце у структурі онкологічної захворюваності чоловічого населення. Ключовим компонентом раннього виявлення раку простати є визначення рівня простатоспецифічного антигену в крові, відомого як ПСА-тест.
Простатоспецифічний антиген був вперше виділений у 1970-х роках і схвалений для клінічного використання як онкомаркер у кінці 1980-х років. З тих пір ПСА-тест став найпоширенішим інструментом скринінгу раку простати, хоча його використання залишається предметом активних дискусій у медичній спільноті.
Біохімія та фізіологія ПСА
Простатоспецифічний антиген є глікопротеїном з молекулярною масою приблизно 34 кілодальтон, який належить до родини калікреїнових протеаз. ПСА продукується епітеліальними клітинами простати і виконує функцію розрідження еякуляту шляхом розщеплення семіногеліну і фібронектину. В нормальних умовах ПСА проникає у кров у незначних кількостях через гематопростатичний бар’єр.
У сироватці крові ПСА існує у декількох формах: вільний ПСА (10-30% від загальної кількості) та зв’язаний з білками-інгібіторами протеаз ПСА (70-90%). Основними зв’язуючими білками є альфа-1-антихімотрипсин та альфа-2-макроглобулін. Співвідношення вільного та загального ПСА має діагностичне значення у диференціальній діагностиці доброякісних та злоякісних процесів у простаті.
«ПСА є органоспецифічним, але не ракоспецифічним маркером,» – підкреслює експерт клініки Спіженка. «Це означає, що підвищення рівня ПСА вказує на патологічні процеси у простаті, але не обов’язково на рак. Саме тому важливо правильно інтерпретувати результати аналізу у контексті клінічної картини.»
Фактори, що впливають на рівень ПСА
Рівень ПСА у сироватці крові може підвищуватися не лише при раку простати, а й при інших станах. Доброякісна гіперплазія простати є найчастішою причиною підвищення ПСА у чоловіків старшого віку. При цьому стані рівень ПСА зростає пропорційно об’єму простати – приблизно на 0,3-0,4 нг/мл на кожен грам тканини залози.
Запальні процеси у простаті, включаючи гострий та хронічний простатит, можуть спричиняти значне підвищення ПСА. Інфекції сечовивідних шляхів, маніпуляції на простаті (біопсія, цистоскопія, катетеризація), фізичне навантаження та навіть їзда на велосипеді можуть тимчасово підвищувати рівень антигену.
Вік є важливим фактором, що впливає на базальний рівень ПСА. Встановлено пряму кореляцію між віком та концентрацією ПСА у сироватці, з очікуваним щорічним приростом приблизно 3,2% у здорових чоловіків віком 60 років. Це призвело до розробки віково-скорегованих нормальних значень ПСА.
Віково-скореговані норми ПСА
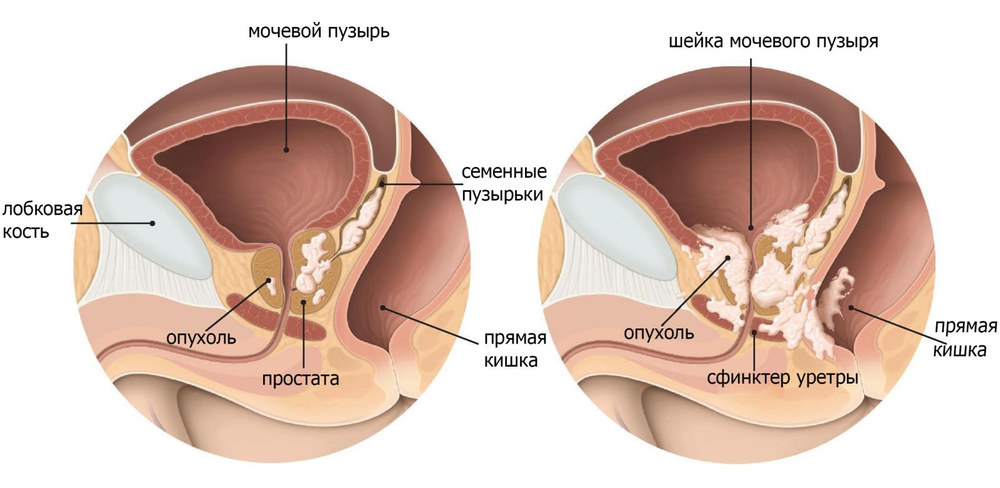
Традиційний поріг 4,0 нг/мл як верхня межа норми не враховує природного збільшення рівня ПСА з віком. Використання єдиного порогового значення може призводити до гіпердіагностики у літніх чоловіків та пропуску раку у молодших. Віково-скореговані референсні значення базуються на 95-му перцентилі розподілу ПСА у здорових чоловіків відповідного віку.
Рекомендовані нормальні значення ПСА за віковими групами:
- 40-49 років: ≤2,5 нг/мл
- 50-59 років: ≤3,5 нг/мл
- 60-69 років: ≤4,5 нг/мл
- 70-79 років: ≤6,5 нг/мл
Ці значення дозволяють більш точно інтерпретувати результати ПСА-тесту та зменшити кількість непотрібних біопсій у літніх пацієнтів при одночасному покращенні виявлення клінічно значущого раку у молодших чоловіків.
Співвідношення вільного та загального ПСА
Одним з способів покращення специфічності ПСА-тесту є визначення співвідношення вільного ПСА до загального (f/t ПСА). При раку простати відносна частка зв’язаного ПСА зростає, що призводить до зниження співвідношення f/t ПСА. Цей показник особливо корисний у пацієнтів з рівнем загального ПСА у «сірій зоні» 4-10 нг/мл.
Співвідношення f/t ПСА менше 0,18 (18%) асоціюється з підвищеним ризиком раку простати та може служити показанням до проведення біопсії. Навпаки, співвідношення більше 0,25 (25%) свідчить про нижчу ймовірність злоякісного процесу. Використання цього параметра дозволяє уникнути до 20% непотрібних біопсій без пропуску клінічно значущого раку.
Сучасні рекомендації щодо ПСА-скринінгу
Рекомендації професійних організацій щодо ПСА-скринінгу еволюціонували протягом останніх десятиліть. Американська робоча група з профілактичних послуг (USPSTF) у 2018 році змінила свою позицію, рекомендуючи індивідуальний підхід до скринінгу для чоловіків віком 55-69 років. Це рішення має прийматися після обговорення потенційних переваг і ризиків з лікарем.
Європейські рекомендації є більш активними щодо скринінгу. Європейська асоціація урології рекомендує ризик-адаптовану стратегію з початковим визначенням ПСА у віці 45 років для чоловіків групи ризику та 50 років для інших. Подальші інтервали скринінгу визначаються базовим рівнем ПСА та індивідуальними факторами ризику.
Останній консенсус Великобританії 2024 року рекомендує проактивний підхід до ПСА-тестування у чоловіків високого ризику, включаючи афроамериканців віком понад 45 років, чоловіків з родинним анамнезом раку простати та носіїв мутацій BRCA2.
Альтернативні біомаркери

Обмеження ПСА-тесту стимулювали розробку нових біомаркерів для покращення діагностики раку простати. Простатичний індекс здоров’я (PHI), який поєднує загальний ПСА, вільний ПСА та про-ПСА, показує кращу специфічність у диференціації раку та доброякісної гіперплазії.
4Kscore є алгоритмом, що враховує чотири калікреїнові маркери разом з клінічними даними для прогнозування ризику агресивного раку простати. Урінарний тест PCA3 та SelectMDx аналізують специфічні РНК-маркери у сечі та можуть використовуватися для стратифікації ризику перед біопсією.
Мультипараметрична МРТ простати набуває дедалі більшого значення як додатковий метод діагностики. Поєднання підвищеного ПСА з підозрілими змінами на МРТ значно підвищує ймовірність виявлення клінічно значущого раку.
Роль ПСА у моніторингу лікування
ПСА відіграє ключову роль не лише у скринінгу, а й у моніторингу ефективності лікування раку простати. Після радикальної простатектомії рівень ПСА повинен знизитися до невизначуваних значень (менше 0,1 нг/мл) протягом 6-8 тижнів. Підвищення ПСА до 0,2 нг/мл або вище після операції визначається як біохімічний рецидив.
При променевій терапії найнижчий рівень ПСА (надир) досягається повільніше, протягом 18-24 місяців. Критерієм біохімічного рецидиву після опромінення є підвищення ПСА на 2 нг/мл порівняно з надиром. ПСА також використовується для моніторингу ефективності гормональної терапії та хіміотерапії при метастатичному раку.
Майбутнє ПСА-скринінгу
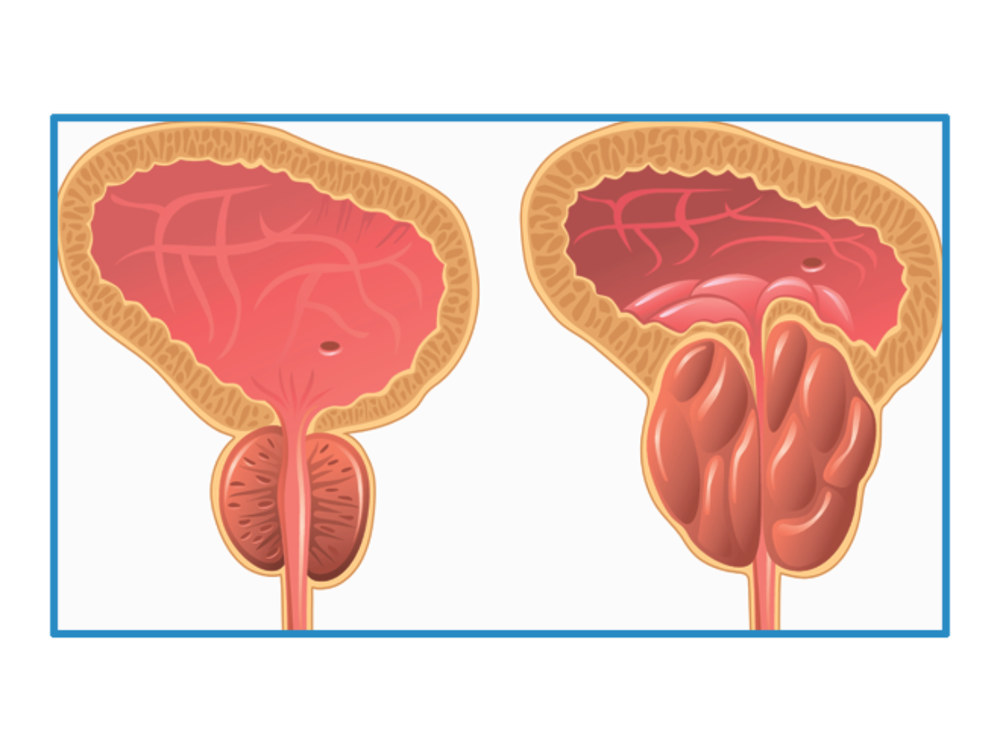
Розвиток персоналізованої медицини передбачає індивідуалізацію підходів до скринінгу раку простати. Інтеграція генетичних маркерів ризику, нових біомаркерів та алгоритмів штучного інтелекту може значно покращити точність скринінгу.
Полігенні індекси ризику, які аналізують сотні генетичних варіантів, можуть допомогти ідентифікувати чоловіків з підвищеним ризиком агресивного раку простати. Поєднання цих індексів з традиційним ПСА-тестом дозволить більш точно стратифікувати ризик та оптимізувати скринінгові стратегії.
ПСА-тест залишається наріжним каменем скринінгу раку простати, незважаючи на свої обмеження. Розуміння фізіології ПСА, факторів що впливають на його рівень, та правильна інтерпретація результатів є критично важливими для ефективного використання цього біомаркера.
Майбутнє скринінгу раку простати лежить у персоналізованому підході, який поєднує ПСА з іншими клінічними та молекулярними маркерами для оптимізації співвідношення користі та шкоди від скринінгу.